สารหนูกับสิ่งแวดล้อม
รศ.ดร. วิโรจน์ บุญอำนวยวิทยา
ดร. นิตินัย ขำมาลัย
สารหนู (arsenic) เป็นธาตุที่มีน้ำหนักโมเลกุล 74.9216
เลขอะตอมเท่ากับ 33 มีวาเลนซ์เท่ากับ 5, 3, 0 และ -3 สารหนูปกติจะมีสีเหลืองหรือสีเทา
สารหนูเป็นสารที่รู้จักกันมานานกว่า 3,000 ปี โดยมีการใช้ในทางการแพทย์และใช้เป็นยาพิษเช่นกัน
ผู้ที่ค้นพบคนแรกคือ Albertus Magnus (1206-1280 BC) |
|
สารหนูโดยปกติสามารถเข้าสู่ร่างกายมนุษย์ได้ทางการหายใจ
การดูดซึมของลำไส้ และผ่านผิวหนัง ความเป็นพิษของสารหนูอย่างรุนแรงเกิดขึ้นได้โดยการดูดซึมผ่านลำไส้
โดยจะมีอาการอย่างไรขึ้นอยู่กับรูปแบบและปริมาณของสารหนู โดยสารหนูปริมาณเพียง
130 มิลลิกรัม จะทำให้สำไส้และตับถูกทำลาย การทำงานของระบบหัวใจผิดปกติและเสียชีวิตได้
ส่วนความเป็นพิษสารหนูแบบเรื้อรัง จะมีผลต่อตับและไตเมื่อได้รับสารหนู
1.4 มิลลิกรัมต่อวันเป็นเวลา 3 อาทิตย์ ข้อมูลที่ได้จากสัตว์ทดลองแสดงให้เห็นว่าสารหนูวาเลนซี
3 มีพิษมากกว่าสารหนูวาเลนซี 5 และสารหนูในรูปของสารละลายจะมีพิษมากกว่าสารหนูที่ไม่ละลาย
ทั้งนี้อาจเนื่องมากจากสารหนูในสารละลายถูกดูดซึมได้ดีกว่า
อย่างไรก็ตาม
ร่างกายสามารถขับสารหนูออกได้เองในเวลา 2-3 วัน เมื่อได้รับสารหนูปริมาณไม่มากนัก
ปริมาณของสารหนูในร่างกายสามารถตรวจพบได้จากปริมาณของสารหนูที่พบได้ในเส้นผมและขน การได้รับสารหนูเป็นเวลานาน อาการทางผิวหนัง จะเริ่มตั้งแต่เกิดอาการระคายเคือง
กลายเป็นด้านหนาที่ผิวหนัง เม็ดสีที่ผิวเป็นสีดำเข้ม อาจพบเป็นรอยตกกระตามร่างกาย
แต่ที่ฝ่ามือจะเป็นจุดขาวๆ เต็มไปหมด ส่วนฝ่าเท้าจะเกิดจุดสีดำใหญ่เห็นได้ชัดเจนทั้งสองฝ่าเท้า
จนกระทั่งถึงกลายเป็นมะเร็งที่ผิวหนังได้ 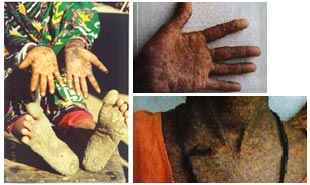
รูปแบบของสารหนูจะพบร่วมกันแร่ทองแดง ตะกั่ว และสังกะสีซัลไฟด์ โดยพบอยู่ในรูปของ
sulfide realgar หรือ orpiment โดยจะพบมากที่สุดในรูปของ arsenopyrite
(FeAsS) ออกไซด์ของสารหนูในรูป arsenic trioxide ส่วนใหญ่จะใช้ในทางการเกษตร
เช่น ยาฆ่าแมลง ยาปราบศัตรูพืช ยาฆ่าเชื้อรา เป็นต้น สารหนูในรูปของธาตุจะใช้เป็นส่วนผสมของโลหะอัลลอยด์
เช่น ผสมกับตะกั่วในแบตเตอรี หรือในรูปของแกลเลียมอาร์เซไนด์ (gallium
arsenide) สำหรับเคลือบสีในนาฬิกาดิจิตอล หรือใช้เป็น light-emitting
diode สำหรับเครื่องมือต่างๆ
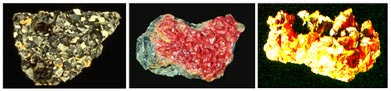 |
Arsenopyrite |
Orpiment |
Realgar |
ธาตุสารที่พบทั่วไปคือเป็นองค์ประกอบของแร่อาร์ซีโนไพไรท์
มีปริมาณตั้งแต่ร้อยละ 0.02 ถึง 0.5 ปริมาณของสารหนูในหินภูเขาไฟอาจพบได้เป็นปริมาณมากถึง
100
มิลลิกรัมต่อกิโลกรัม หรือในอัตราเฉลี่ย 2-3 มิลลิกรัมต่อกิโลกรัม
ส่วนในหินตะกอน เช่น หินภูเขาไฟ หินปูน หินทราย พบสารหนูจำนวนน้อยมาก
และในแหล่งแร่มังกานีส
อาจพบมากถึง 15,000 มิลลิกรัมต่อกิโลกรัม สารประกอบซัลไฟด์ของสารหนูสามารถถูกเติมออกซิเจนได้ง่าย
เมื่อสัมผัสกับอากาศจะกลายเป็นเกลืออนินทรีย์ของสารหนู (inorganic
arsenic salt) ซึ่งมีคุณสมบัติละลายน้ำได้ดี นอกจากจะพบในแร่แล้ว
สารหนูยังถูกพบในสิ่งอื่นๆ เช่น ในน้ำตามธรรมชาติมีอยู่ในอัตราความเข้มข้น
1-2 ไมโครกรัมต่อลิตร
จนถึงมากกว่า 5,000 ไมโครกรัมต่อลิตร สารหนูความเข้มข้นสูงจะพบได้มากในน้ำใต้ดิน
ในบางพื้นที่ บ่อน้ำใต้ดินไม่สามารถใช้การได้เนื่องจากความเป็นพิษของสารหนูสูงมาก
เช่น ในประเทศอาร์เจนตินา (1-7500 ppm) ชิลี (100-1000 ppm)
เมกซิโก (8-620
ppm) จีน (40-750 ppm) ฮังการี (2-176 ppm) อินเดีย (10-3200
ppm) บังคลาเทศ (0.5-3500 ppm) และเวียดนาม (1-3050 ppm) (Smedley,
2002) 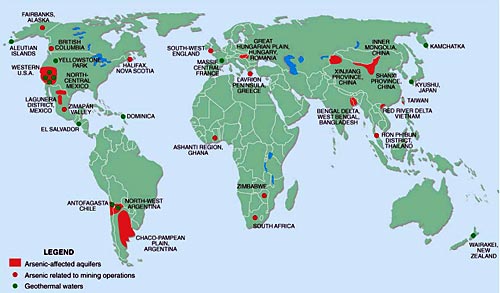
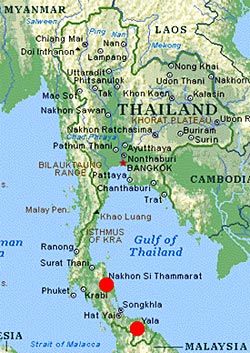
สำหรับในประเทศไทย ได้มีรายงานการพบสารหนูในบ่อน้ำใช้บริโภค
บริเวณอำเภอร่อนพิบูลย์ จังหวัดนครศรีธรรมราช ในปี พ.ศ. 2530 และอำเภอบันนังสตาร์
จังหวัดยะลา สารหนูที่พบเป็นสารหนูที่ปนเปื้อนในดิน มีปริมาณตั้งแต่
21-16,000
มิลลิกรัมต่อกิโลกรัม (Visoottiviseth, 2002) สารหนูที่พบในอำเภอร่อนพิบูลย์ส่วนใหญ
่อยู่ร่วมกับสายแร่ดีบุก
โดยสารหนูจะอยู่ในรูปของ arsenopyrite (FeAsS) หรือในรูปอื่นซึ่งมีซัลไฟด์เป็นองค์ประกอบ
การแพร่กระจายของสารหนูในพื้นที่ เกิดจากกิจกรรมการทำเหมืองแร่ดีบุก ทำให้สารหนูในรูปอาร์ซีโนไพไรต์
ที่ปนอยู่กับสายแร่ถูกขุดออกมาด้วย ในกระบวนการแยกแร่ออก อาร์ซีโนไพไรต์ถูกแยกออกมากับหางแร่และทิ้งไว้
ทำให้เกิดการออกซิเดชันกับอากาศ
และน้ำทำให้สารหนูที่อยู่ในแร่ แพร่กระจายออกมาสู่แหล่งน้ำ
บริเวณที่จัดว่าอยู่ในกลุ่มความเสี่ยง
ได้แก่ เหมืองแร่ถ่านหิน ดีบุก ทองคำ ตะกั่วและเงิน ที่ปิดทำเหมือง และไม่ได้มีการจัดการเหมืองแร่ที่ดี
ไม่มีการจัดเก็บกากแร่ มีการปล่อยทิ้งไว้ให้สัมผัสกับน้ำ และอากาศ
ซึ่งเร่งให้เกิดการสลายตัวของแร่ที่มีสารหนู เป็นองค์ประกอบหรือโลหะต่างๆ
เช่น ตะกั่ว ปรอท ปนเปื้อน และแพร่กระจายไปตามแหล่งน้ำต่างๆ |
 |
สารประกอบซัลไฟด์ของสารหนูนี้ ปกติจะไม่ละลายหรือละลายได้น้อยมาก แต่เมื่อได้รับความร้อนความชื้น
และอากาศจากธรรมชาติ จะสามารถเกิดปฏิกิริยาเคมี เปลี่ยนแปลงไปเป็นสารประกอบออกไซด์
ซึ่งละลายน้ำได้ดี
| FeAsS -> FeS + As |
| 3O2 + As -> 2As2O3 |
| As2O3 - > H3AsO3 (ortho arsenous acid) |
| |
-> H4As2O5 (pyro arsenous acid)
-> HAsO2 (meta arsenous acid) |
และในบางครั้งก็สามารถเกิดการออกซิเดชันกำมะถัน กลายเป็นกรดกำมะถันซึ่งสามารถละลายเหล็กและโลหะอื่นๆ
ลงในน้ำ นอกจากนั้น กรดอาร์ซีนัสที่เกิดขึ้นยังสามารถรวมตัวกับอิออนของโลหะกลายเป็นเกลืออาร์ซีไนต์ซึ่งละลายน้ำได้ดี
แต่ในบางครั้ง เกลือที่เกิดขึ้นก็เป็นตะกอน เช่น การตกตะกอนร่วมกับอิออนของเหล็ก
(3+) จะเห็นได้ว่าปริมาณสารหนูในน้ำสามารถที่จะเกิดการเปลี่ยนแปลงได้
ทั้งในแง่ที่ลดลง และเพิ่มขึ้นได้เองตามธรรมชาติ อย่างไรก็ตาม ปฏิกิริยาทางเคมีที่เกิดขึ้นนี้จะช้ามาก ซึ่งถ้ามีแบคทีเรียอยู่
ปฏิกิริยาจะถูกเร่งถึง 106 เท่า (Silverman and Ehrlich,1964) โดยแบคทีเรียจะเร่งปฏิกิริยาให้เหล็ก
(2+) ถูกออกซิไดซ์เป็นเหล็ก (3+) (Barrett,1990) ตามสมการ
FeAsS + 11Fe(III) -> 12Fe(II) + As(III) + S(VI) แบคทีเรียชนิด sulfur-oxidizing bacteria สามารถออกซิไดซ์ซัลเฟอร์ในแร่อาร์ซีโนไพไรต์ได้
ได้แก่ Thiobacillus ferrooxidans เป็นแบคทีเรียจำพวก mesophile และ acidophile
เป็นประเภทแกรมลบ รูปร่างเป็นท่อนสั้นขนาด 0.5x1.5 ?m โคโลนีมีรูปร่างกลมขนาดเส้นผ่านศูนย์กลางประมาณ
0.1-0.2 มิลลิเมตร ตรงกลางมีวงสีส้มของสนิมเหล็ก สามารถเจริญเติบโตในสภาวะที่มีอากาศ
ดำรงชีพแบบ lithotrophs และ autotrophs โดยสามารถออกซิไดซ์เหล็กเฟอร์รัส
แต่ไม่สามารถใช้สารประกอบอินทรีย์คาร์บอนได้

แบคทีเรียชนิด Thiobacillus ferrooxidans
บรรณานุกรม
1. Barrett, J., Ewart, D.K., Hughes, M.N., Nobar, A.M. and
Poole, R.K., (1989), Biohydrometallurgy, 89, 49.
2. Silverman, M.P. and Ehrlich, H.L., (1964), Advan. Appl.
Microbiol., 6, 153.
3. Visoottiviseth, P., Francesconi, K. and Sridokchan, W.,
(2002), Environmental Pollution, 118, 453–461.
|


